안녕하세요!
지난 시간에는 동적광산란, DLS를 이용한 나노입자의 크기 분석에 대해서 알아보았었습니다.
2023.04.13 - [공부할 시간/분석장비] - DLS (Dynamic Light Scattering), 동적 광산란 - 나노입자의 사이즈 분석
위 글에서, DLS가 입자의 움직임을 측정해서 사이즈에 대한 정보를 알아낸다고 말씀드렸었는데요.
이렇게 용액 내에서 입자의 움직임을 측정해서 알아낼 수 있는 정보가 또 하나 있습니다.
바로 입자의 표면전하이지요.
오늘 다룰 내용은 입자의 표면전하를 분석하는 방법 중 하나인, 제타전위, 제타포텐셜, Zeta potential 분석입니다.
제타 전위는 용액 내 입자의 분산도를 평가, 이해하는 데에 중요한 지표이며,
수처리, 반도체, 의학, 제약, 화학 등 다양한 분야에 널리 이용되는 분석입니다.
입자의 표면 전하
용액에 나노입자 혹은 마이크로입자가 고르게 분산되어 있는 것을 콜로이드, Colloid라고 합니다.
혹은 분산액, dispersion으로도 불립니다.
그리고 이러한 콜로이드 용액 내에 분산되어 있는 입자를 콜로이드 입자라고 합니다.
콜로이드 용액 내에 입자들이 가라앉거나 뭉쳐지지 않고 안정적으로 존재하기 위해서는
입자의 표면 전하 (surface charge)가 중요한 역할을 하게 됩니다.
+) 표면전하 외에도, 입자의 크기, 용액의 pH와 점도 등도 콜로이드의 안정성에 영향을 주는 중요한 요소들입니다.
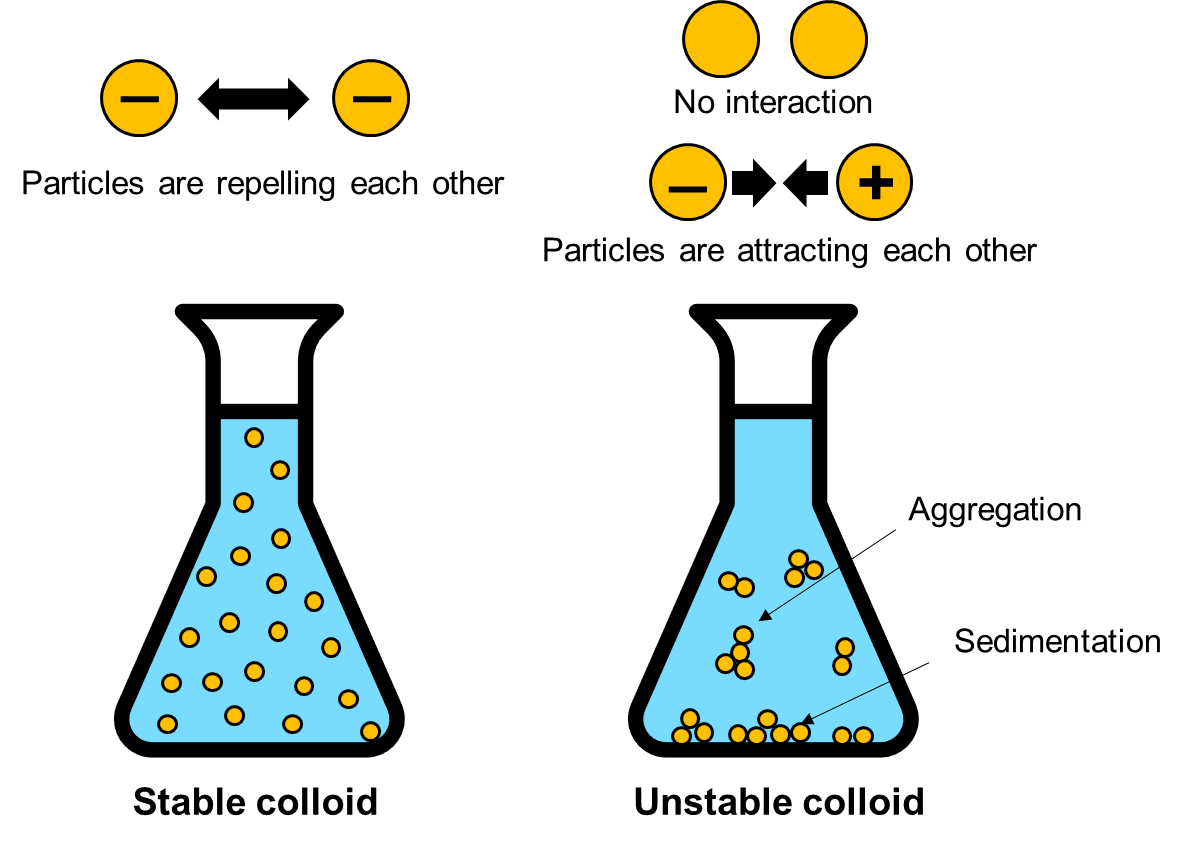
위 그림을 보시면
왼쪽 콜로이드 입자의 경우, 서로 같은 음전하를 띄고 있기 때문에 입자 간에 반발력이 작용하게 되어
콜로이드 입자들이 뭉치지 않고 용액 내에 안정적으로 고르게 분포되어 있을 수 있습니다.
하지만 오른쪽 콜로이드 입자들의 경우,
입자의 표전전하가 약해서 입자간의 반발력이 없거나
입자들이 반대의 전하를 띠고 있어, 오히려 서로 끌어당기는 힘이 발생하게 되어
입자들이 뭉치는 aggregation이 생기게 되고, 결국 침전물 (sedimentation)로 가라앉게 됩니다.
이렇게 입자의 표면 전하는 콜로이드 용액의 안정성을 결정하는 매우 중요한 특성이기 때문에,
입자의 표면전하를 목적에 맞게 조절하여
입자가 용액 내에 안정적으로 분산될 수 있게 하거나
혹은
입자끼리 일부러 뭉치게 만들어서 침전을 유도할 수 있습니다.
입자의 제타 전위, Zeta potential
입자가 용액에 분산되어 있을 때,
입자가 가지는 전하에 의해서 용액 내의 상대이온(counter ion)들이 입자에 흡착되게 됩니다.

위 그림과 같이, 음전하를 띠는 입자가 용액에 분산되어 있는 경우를 예시로 살펴보겠습니다.
음전하를 띠는 입자를 용액 속에 분산시키면,
용액 내에 존재하는 상대이온(counter ion)들이 입자의 전하를 상쇄시키기 위해서 입자 주변에 흡착되게 됩니다.
이렇게 흡착된 상대이온들은 입자와의 거리에 따라서 확산적으로 분포하게 되며
입자 주변에 기존의 용액과 구분되는 전기이중층 (Electrical double layer)을 형성하게 됩니다.
전기적 이중층은 고정층 (Stern layer)과 확산층 (Diffuse charge layer) 두 가지로 구분될 수 있습니다.
고정층이란, 상대이온들이 강하게 흡착되어 상대적으로 움직이지 않는 층을 말하며
확산층은 상대이온이 상대적으로 적어, 전위가 급격하게 낮아지는 층을 의미합니다.
이때, 우리는 입자 주변의 액체를 크게 두 가지 영역으로 나눌 수 있는데요.
먼저, 입자에 흡착되어 있는 액체층과 → 전기이중충 내부
입자에 흡착되어있지 않고 자유롭게 움직이는 액체 → 전기이중충 외부
이렇게 두 가지 영역으로 구분을 했을 때,
이 두영역의 경계면, 즉 전기이중층 최외곽의 경계면을 따라서 입자가 움직이기 때문에,
이 경계면을 미끄러지는면 (Slipping plane)이라고 정의하고,
미끄러지는 면에서의 전위를 제타전위라고 합니다.
용액 내의 입자의 움직임을 분석해서 제타전위를 측정하면 입자의 표면전하를 간접적으로 알 수 있습니다.
제타전위의 절댓값이 클수록 콜로이드 용액은 높은 안정성을 가질 수 있으며,
일반적으로 입자가 ± 30 mV 보다 큰 제타전위를 가져야 용액 내에 안정적으로 분산될 수 있습니다.
제타 전위 측정
제타 전위는 전기영동 이동성(electrophoretic mobility)을 측정하여 얻을 수 있습니다.
전기영동(Electrophoresis)이란,
전극사이의 전하장의 영향 아래에서 용액 속의 전하를 띤 입자가 반대 전하의 전극을 향하여 이동하는 현상을 말합니다.
제타 전위를 측정하기 위해서 사용되는 셀은 아래와 같이 생겼습니다.

셀 양옆에는 전기장을 형성시킬 수 있는 전극이 있고
내부에는 분석하고자 하는 용액이 위치할 공간이 있습니다.
분석을 위해서 셀 안에 용액을 넣고 이를 제타전위 측정장비에 넣은 뒤에 분석을 시작하면
용액 내부에 전기장이 걸리게 되고, 전하를 띤 입자들이 전기장에 반응하여 움직이게 됩니다.
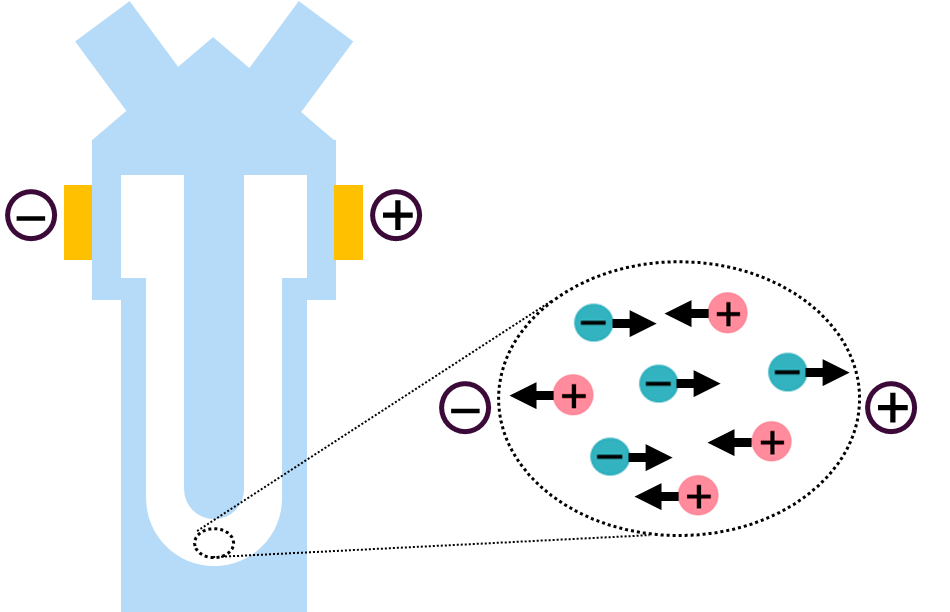
이때, 입자가 움직이는 속도는 입자의 제타전위 값에 비례하게 되는데요.
입자의 제타 전위 절댓값이 크면, 입자는 빠르게 이동하고
입자의 제타 전위 절댓값이 작으면, 입자는 천천히 이동합니다.
입자의 이동속도를 알아내기 위해서는 도플러 시프트 (Doppler frequency shift of the scattered light)를 이용합니다.
이를 좀 더 자세히 설명하자면,
용액 내부에서 이동 중인 입자에 레이저를 조사하면 산란광이 발생하게 되는데
이때 산란광의 주파수(frequency)는 입자의 이동속도에 따라 변화하기 때문에
이러한 산란광의 주파수 변화를 측정하여 입자의 이동 속도를 알아낼 수 있습니다.
이렇게 알아낸 입자의 이동속도와
용매의 굴절률, 유전상수, 점도 등의 정보를 함께 이용하면
최종적으로 입자의 제타전위 값을 알아낼 수 있습니다.
제타 전위에 영향을 미치는 인자들
pH
제타전위는 pH에 따라 달라질 수 있습니다.

카복실기(carboxyl group)와 아민기(amine group)를 표면에 가지고 있는 입자를 예시로 살펴봅시다.
카복실 그룹을 가진 입자의 경우,
낮은 pH 조건에서는 카복실기가 H+ 이온과 결합하여 중성을 띠게 되지만
높은 pH 조건에서는 카복실기가 H+을 잃고 음이온의 형태를 갖게 되기 때문에 입자는 음전하를 띠게 됩니다.
아민기를 가진 입자의 경우,
낮은 pH 조건에서는 아민기가 H+ 이온과 결합하여 전체적으로 입자는 양전하를 띠게 되고
높은 pH 조건에서는 H+을 잃고 중성을 띠게 됩니다.
다시 한번 정리해 보자면, pH 변화에 따라 입자의 표면전하와 제타전위가 변화할 수 있으며,
일반적으로 낮은 pH에서 높은 pH 조건으로 변화할수록 입자의 제타전위는 감소하게 됩니다.
그리고 이렇게 제타전위가 변할 때,
제타전위의 값이 0이 되는 지점을 등전점 (Isoelectric point)이라고 합니다.

등전점은 물질에 따라 다르며,
일반적으로 콜로이드 용액이 등전점 근처의 pH 조건을 갖게 되면
제타전위의 절댓값이 낮기 때문에 용액 안의 입자끼리 응집이 발생하기 쉽게 되어 낮은 안정성을 보이게 됩니다.
용액의 전도도 (Conductivity)
용액의 전도도는 용액의 이온세기 (ionic strength)를 나타내는 지표입니다.
콜로이드 용액에 NaCl과 같은 염(salt)이 녹아있다면 용액의 전도도와 이온세기가 증가합니다.
※ 용액 내 염의 농도가 높다. = 용액의 이온세기가 크다. = 용액의 전도도가 높다.
콜로이드 입자 주위에 형성되는 전기이중층의 두께는 용액 내부의 이온 농도에 영향을 받기 때문에
용액이 높은 이온세기 (ionic strength)를 갖는 경우에는 입자의 전기이중층이 압축되게 되고 제타전위가 감소합니다.
또한 아주 용액 내 염의 농도가 아주 높은 경우에는 전기이중층이 붕괴되어 입자들이 응집될 수 있습니다.
농도
제타 전위를 분석할 때에, 입자의 농도 또한 결과에 영향을 미치게 됩니다.
샘플의 농도가 너무 낮거나, 높으면 정확한 제타전위값을 얻을 수 없으므로
장비가 측정가능한 농도를 확인한 뒤에 적절한 농도의 샘플을 준비하는 것이 중요합니다.
오늘은 입자의 표면전하 및 제타전하와 이를 분석하는 방법에 대해서 알아보았습니다.
다음번에도 또 다른 유익할 만한 내용을 가지고 찾아오도록 하겠습니다.
여기까지 읽어주셔서 감사합니다.
좋은 하루 보내세요!
-엠마리-




댓글